日本インターフェロン・サイトカイン学会にて発表しました!
2019.09.06
学会・論文
2019年8月2、3日に兵庫県神戸市にて開催された「第84回日本インターフェロン・サイトカイン学会」にて、アサイゲルマニウムのインフラマソーム活性抑制効果について発表いたしました。
<発表の概要>
日時 :2019年8月2日(金)
発表番号:P-15
場所 :神戸国際会議場
演題名 :有機ゲルマニウム化合物Ge-132によるATPとの錯体形成を介したインフラマソーム活性抑制効果
発表者 :㈱浅井ゲルマニウム研究所 研究部 安積遵哉
<はじめに>
◆インフラマソームとは・・・?
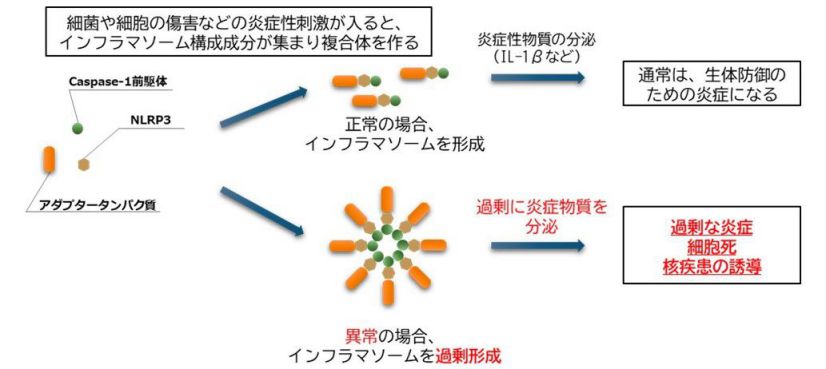
自然免疫系の細胞が持っているタンパク複合体で、細菌やウイルス感染、細胞の傷害など、身体にとって危険な信号をキャッチしたときに形成されて、生体防御のための炎症反応を起こしています。
このようにインフラマソームによる炎症は、私たちの身体に必要なシステムですが、インフラマソームが活性化しすぎると過剰な炎症が起き、動脈硬化や痛風、肝硬変やアルツハイマー型認知症などの発生に関係すると言われています。
◆本研究テーマの背景
近年、エネルギー物質として知られる「ATP」が、細胞が傷つくことによって漏れ出るとそれが刺激となり、インフラマソームを過剰形成(=活性化)し、炎症を起こすことがわかってきました。
当社では以前、アサイゲルマニウム(AG)と生体成分であるATPが錯体形成する(くっつく)ことを論文発表しています。このことから、アサイゲルマニウムはATPと錯体形成することによりインフラマソームの形成を抑制するのではないかと考え、本研究に至りました。
<研究の内容>
◆アサイゲルマニウムによって炎症促進物質の分泌が抑えられる
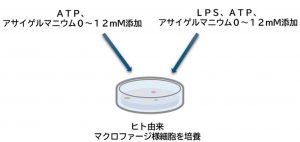
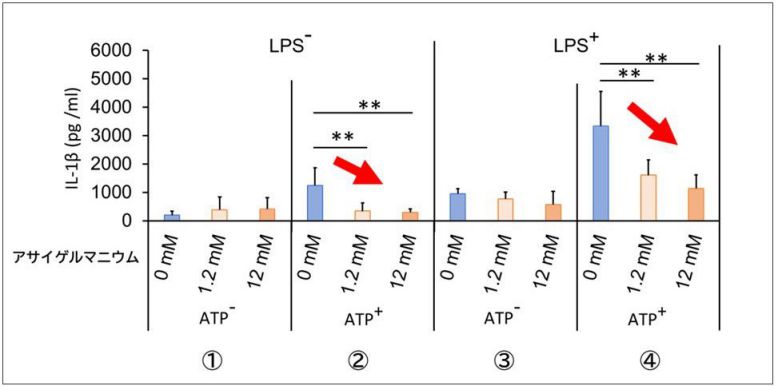
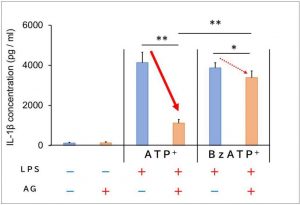
① ATP添加無し、LPS添加無し : IL-1βは増えない。
② ATP添加有り、LPS添加無し : IL-1βが分泌される(アサイゲルマニウム0mM)。
しかし、アサイゲルマニウムを添加することで濃度依存的にIL-1βの分泌が抑えられる。
③ ATP添加無し、LPS添加有り : LPSが刺激となり、IL-1βの分泌がやや増える。
④ ATP添加有り、LPS添加有り : IL-1βが分泌される(アサイゲルマニウム0mM)。
しかし、アサイゲルマニウムを添加することで濃度依存的にIL-1βの分泌が抑えられる。
実験の結果、ATPを添加することで炎症物質であるIL-1βの分泌が増加しましたが、アサイゲルマニウムを加えることでその量が減少しました。(②)
またLPSを添加すると、よりIL-1βの分泌が増加しますが、その条件下でもアサイゲルマニウム添加でその量が減少していることが明らかになりました。(④)
これは、アサイゲルマニウムが炎症の原因物質の分泌抑制に関与していることを示しています。
◆アサイゲルマニウムはATPと錯体形成する(くっつく)ことで炎症を抑制する
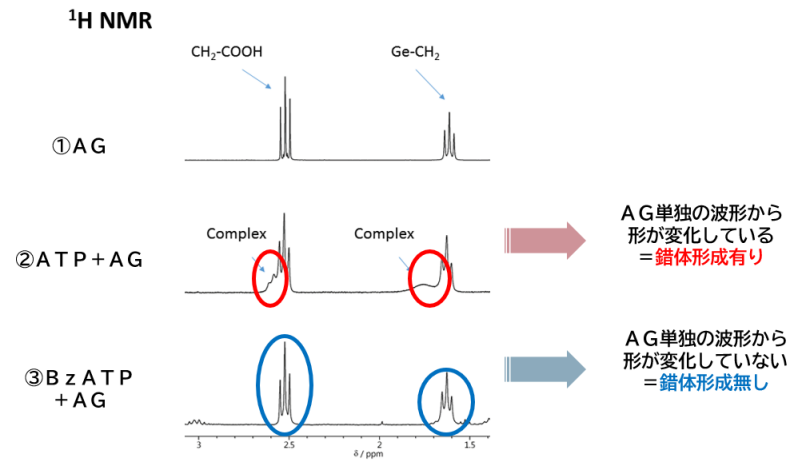
アサイゲルマニウムは、ATPと錯体形成する(くっつく)ことが明らかにされていますが、改めて錯体形成を確認するため、アサイゲルマニウムとATPを混合し、NMRという分析機器を使用し測定しました。
① アサイゲルマニウム(AG)単独の波形を確認する。
② ATPとアサイゲルマニウム(AG)の混合したものの波形を確認する。
③ ATPと形が似ているBzATP(構造的にAGと錯体形成しないと推測される)の混合したものの波形を確認する。
◆アサイゲルマニウムはインフラマソーム活性上昇によって起こる細胞死(パイロトーシス)を抑制する
正常な細胞がウイルス感染などを起こした場合、インフラマソーム活性を上昇させて細胞死を誘導することが知られています。細胞死には様々な種類がありますが、インフラマソームの活性上昇によって引き起こされる「パイロトーシス」に着目し、アサイゲルマニウムによるパイロトーシスの抑制について実験しました。
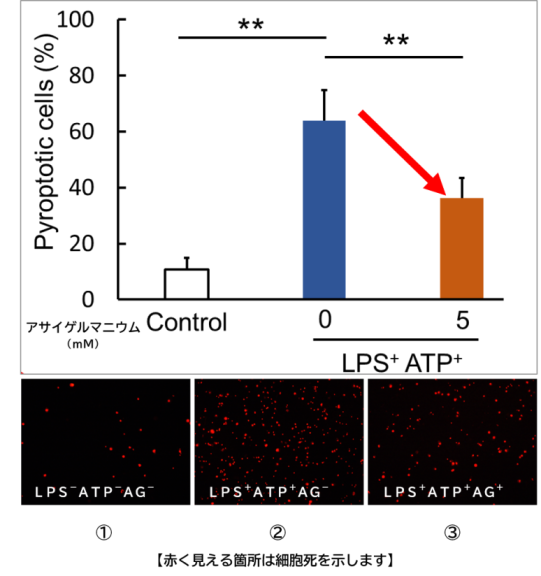
① 通常状態
② LPS、ATPを添加することでインフラマソーム活性上昇によって「パイロトーシス」が誘導される。
③ LPS、ATPに加えて、アサイゲルマニウムを添加すると、②と比べ、「パイロトーシス」を抑制。
実験の結果、アサイゲルマニウムを添加することでパイロトーシスが抑制されることが明らかになりました。
<結論・まとめ>
これまで、アサイゲルマニウムが炎症を抑制するという報告は多数ありましたが、そのメカニズムについては明らかにされていませんでした。
本研究では、アサイゲルマニウムがインフラマソーム形成の引き金となるATPとの錯体形成を介して、炎症の大元となるインフラマソームの形成を抑制することがわかりました。
更にはインフラマソーム活性化による細胞死(パイロトーシス)まで抑制することが明らかになりました。
本研究により、アサイゲルマニウムはインフラマソーム活性が関係する動脈硬化や痛風、2型糖尿病、肝硬変、アルツハイマー型認知症などの炎症性疾患に対して役立つ可能性が示唆されました。