「痛い!」と感じることは、私たちの身体に何かしらの異変が生じていることを知らせる重要なサインです。
切り傷や火傷を負ったりして組織が傷つけられると、その部位の周辺から「発痛物質(神経伝達物質)」が漏れ出し、それが電気信号に変換され、末梢神経から感覚神経などを伝い、脳に伝達され「痛み」を認識しています。
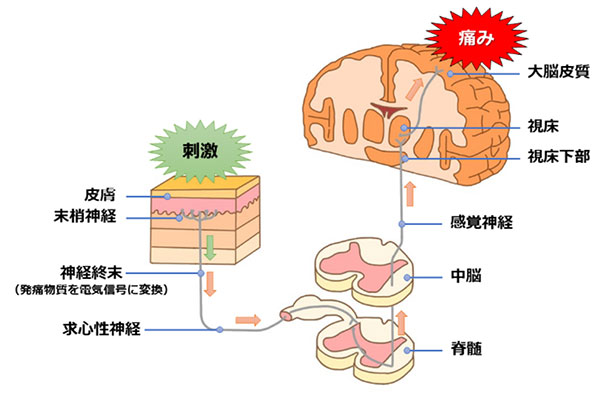
また、痛みと言っても日常的な外傷による痛みや頭痛等の痛みから、病気になって初めて経験する痛みまで、その原因や状態は様々で複合的です。全ての「痛み」を明確に分類することはできませんが、主に以下のように分類されています。
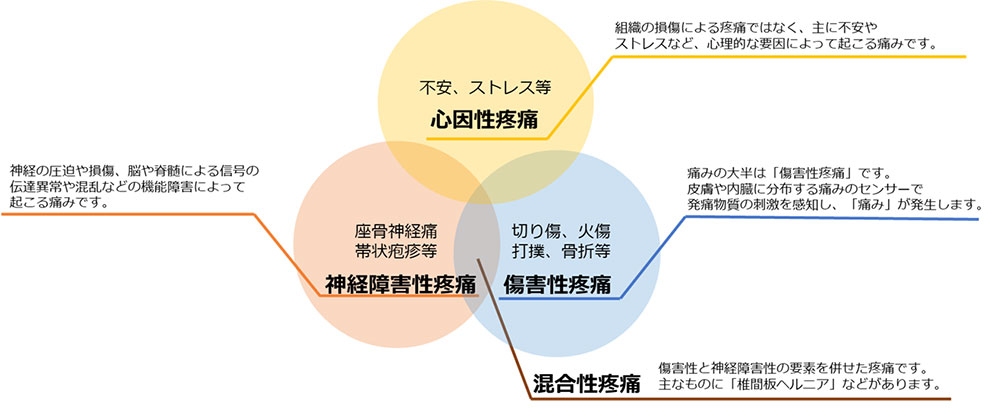
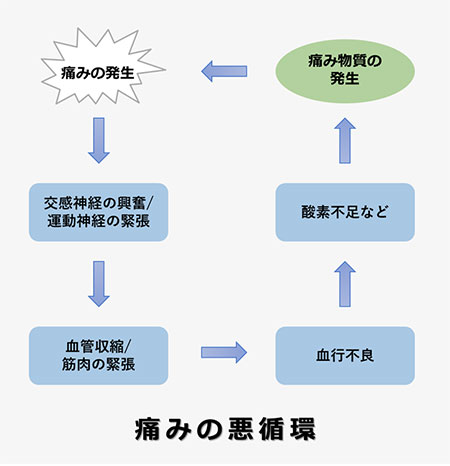
痛みは、交感神経や筋肉の緊張を招き、血圧上昇、心拍数増加、血管収縮、呼吸回数の増加など、循環器系や呼吸器系にとっても大きな悪影響をもたらします。
「痛み」を感じた時、すぐに処置し改善することが望ましいですが、我慢し、放置するとさらに新たな痛みを生む「痛みの悪循環」に陥ってしまい、慢性的な痛みとなり、苦痛な状態が長引くことになってしまいます。
ここでは、「痛み」に対するアサイゲルマニウムの作用研究についてご紹介します。
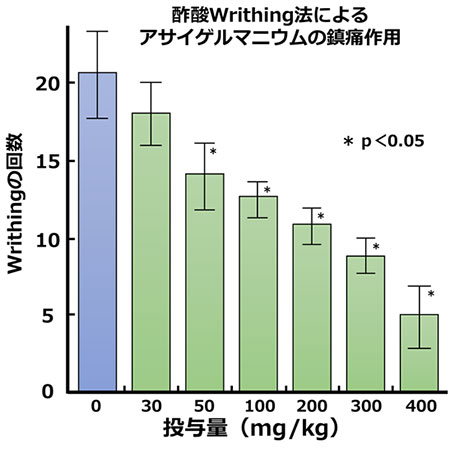
マウスの皮下に体重1kgあたり30~400mgのアサイゲルマニウムを1回投与した後、30分後に痛みを引き起こす物質(0.7%の酢酸-生理食塩液)を腹腔内に投与し、5分後から10分間に起こるwrithing回数(痛みにより身をよじる回数)を測定しました。
アサイゲルマニウムを投与していない群と比較して、アサイゲルマニウムを投与した群は投与量が多くなるに従って、writhing回数が抑制され、鎮痛効果があることが確認されました。
鎮痛剤であるモルヒネやペントシジンとアサイゲルマニウムを併用すると、有意に鎮痛作用が増強されることも確認されています。
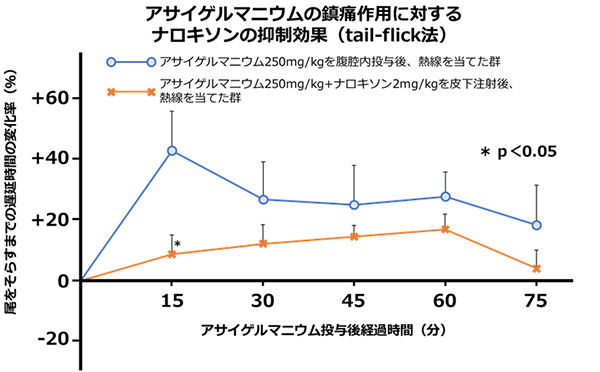
ラットにアサイゲルマニウム250mg/kgを腹腔内投与した群、アサイゲルマニウム250mg/kg +ナロキソン2mg/kgを5分前に皮下注射した群に対してTail-flick法(尾に熱線を当てて刺激する方法)を用いて鎮痛作用を検討しました。
アサイゲルマニウムだけを投与したラット群は、熱による痛みから尾をそらす(反応する)までの時間が遅くなり、鎮痛作用が確認されました。一方、ナロキソン※を併用した群は、尾をそらすまでの時間が早まり、アサイゲルマニウムの鎮痛作用が抑えられることがわかりました。
鎮痛薬の中にはモルヒネのように、オピオイド受容体というタンパク質に作用する麻薬性鎮痛薬(オピオイド)がありますが、オピオイドには体内で作られるものもあります。そのため、アサイゲルマニウムは体内にある鎮痛システムである内在性オピオイド系の活性化を介して鎮痛作用を示していると考えられます。
※ナロキソン:モルヒネ等の過剰な作用を抑える物質。オピオイド拮抗薬。
がん患者は痛みを感じることが多く、早期でも30%の方が、末期がんになると70%の方が痛みを感じるといわれています。
多施設の共同研究による二重盲検比較試験※により切除不能な肺がん患者に対して、痛み(疼痛)や食欲不振、全身倦怠感等の自覚症状について以下の2群について調べました。
①アサイゲルマニウムを1日あたり50mg/kgを基準として摂取した群
②プラゼボ群(アサイゲルマニウムを含まないものを摂取した群)
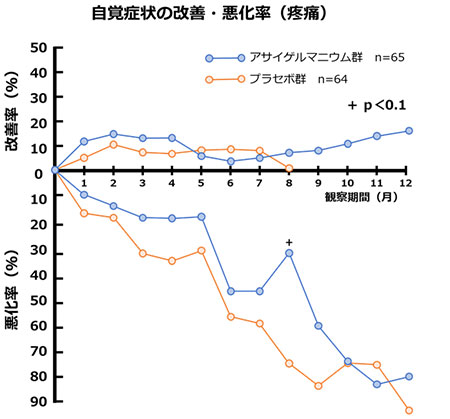
疼痛に対する改善率の推移は、アサイゲルマニウム群の方がやや高い傾向となりました。また、悪化率ではアサイゲルマニウム群で有意に悪化率が軽減されています。同時に実施された「食欲不振」及び「全身倦怠感」に対する評価でも、アサイゲルマニウムを摂取することで有意に改善されている事が明らかになっています。
※二重盲検比較試験:医師にも患者にも、試験の結果が出るまで投与群の内容を知らせずに比較する試験
アサイゲルマニウムは、基礎試験及び臨床試験で「痛みによるつらさ」を軽減する鎮痛作用があることが明らかになっています。そのメカニズムのひとつとして、体内で作られるオピオイド系鎮痛システムの活性化を介して、痛みを抑制している可能性が示されました。一方で、アサイゲルマニウムには麻薬性鎮痛薬であるモルヒネのような意識混濁や依存性、便秘などの副作用がみられないこともわかっています。
「痛み」と「アサイゲルマニウム」の研究は、現在も継続して行われています。